Акролеин
CH2=CH-COH
акриловый альдегид, пропеналь,
G-4 [амер.], Papite [фран]
Акролеин — это бесцветная, легко воспламеняющаяся жидкость с резким, раздражающим запахом. кипящая при 52,5ºC. Жиры животного и растительного происхождения являются сложными эфирами глицерина и жирных кислот. При нагревании жиров, образующийся глицерин дегидратируется с выделением акролеина — это он виновник всем известного раздражающего запаха пригоревшего жира. От двух латинских слов 'acris' (острый, едкий) и 'oleum' (масло) акролеин и получил свое название.
Считается, что акролеин впервые синтезировал австрийский химик Й. Редтенбахер (J. Redtenbacher,) в 1843 году путем сухой перегонки жиров. Однако, намного раньше, ещё в 1779 году шведский химик К. В. Шееле (C.W. Scheele) испытал на себе слезоточивое действие акролеина. Однажды, Шееле поручил своему помощнику перегонку глицерина с водоотнимающим средством, а вернувшись через некоторое время в лабораторию, он обнаружил своего коллегу лежащим без сознания на полу. Страдая от удушья и слез, заливавших лицо, химику удалось вытащить пострадавшего на свежий воздух, где через несколько часов он полностью пришел в себя[13].
В 1885 году, наученные горьким опытом предшественников, Э. Фишер (E. Fischer) и Ю. Тафель (J. Tafel) решили всю работу по синтезу акролеина проводить на открытом воздухе. Казалось, что все меры безопасности были учтены и поначалу все шло просто отлично — из огромного котла через холодильник отогнанный акролеин поступал в приемник, а небольшое количество паров относило ветром. Но однажды, ветер ненадолго сменил направление и этого оказалось достаточно, чтобы Ю. Тафель, находившийся в этот момент около дистиллятора, потерял сознание. К счастью, подоспевший вовремя Фишер, сразу вызвал врачей и отправил друга в больницу. Только через несколько дней Тафель полностью пришел в себя и смог вернуться к работе[19].
Первым, кто предложил использовать акролеин в качестве химического оружия, был шотландский химик У. Рамзай (W. Ramsay) ещё во времена русско-японской войны (1904–1905), но из-за того, что исходный продукт для его синтеза — глицерин был более необходим в производстве взрывчатых веществ, военное министерство Великбритании было вынуждено отклонить его предложение[12].
Не только акролеин, но и многие другие низкомолекулярные альдегиды обладают выраженным раздражающим действием на слизистые оболочки. Первым из альдегидов, который пытались использовать в качестве раздражающего отравляющего вещества, был формальдегид HCHO, а точнее его полимерная форма — параформальдегид, при нагревании которого образуется исходный мономер. В 1906–1909 годах германский военно-морской флот провел ряд экспериментов, в ходе которых при подрыве емкости с параформальдегидом, в замкнутом пространстве удавалось создать концентрацию формальдегида, достаточную, чтобы вызвать слезотечение у испытуемых[10]. В 1912 году один из ведущих немецких военных химиков Альбрехт Шмидт подал патентную заявку на использование формалина, параформальдегида и других ирритантов в пистолетных патронах[11].
 Французская граната Suffocante 1916 |

Чарльз Муре (слева) и Шарль Р. Дюфресс (справа) в химической лаборатории (Париж, 1923 год) |
Через 10 лет французскому химику Чарльзу Муре (Charles Moureu) удалось реализовать идею применения акролеина в качестве боевого отравляющего вещества. Работая над своей докторской диссертацией, посвященной акриловой кислоте, он часто имел дело и с ее «ближайшим родственником» — акролеином и ему хорошо был знаком его непереносимый раздражающий запах. К тому же Ч. Муре знал, что для его промышленного производства не потребуются дефицитные в военное время бром или йод, что выгодно отличало акролеин от других лакриматоров того времени.
До экспериментов Ч. Муре, акролеин получали нагреванием глицерина с водоотнимающими средствами, но из-за небольшого выхода конечного продукта эти методы были непригодны для промышленного производства будущего ОВ[1]. Муре удалось повысить выход акролеина до 60–70% от теоретического, применив в качестве дегидратирующего средства смесь бисульфата калия и сульфата натрия. Но оставалась еще одна проблема, акролеин, даже очищенный, очень быстро окисляется, образуя через несколько дней аморфную массу или смолу — «дизакрил». Ч. Муре решил и эту проблему, он случайно обнаружил, что в присутствии следов многоатомного фенола, акролеин может сохранять свои свойства долгое время. Добавление резорцина или пирогаллола (0,05–0,2%) в качестве антиоксидантов позволяет хранить акролеин месяцы и даже годы[2]. В январе 1916 года французская армия впервые применила акролеин на поле боя.
Кроме Ч. Муре вопросами боевого применения акролеина занимался еще один французский химик — Адольф ЛеПап (Adolphe LePape), в честь которого акролеин получил свое кодовое имя Papite. Если быть точным, то Papite называли смесь акролеина с хлоридом титана. Хлорид титана служил дымообразователем, помогающим корректировать артиллерийский огонь, образуя небольшое облако в месте падения снаряда[8]. Всего в Первую мировую войну во Франции было произведено 183 тонны акролеина[7].
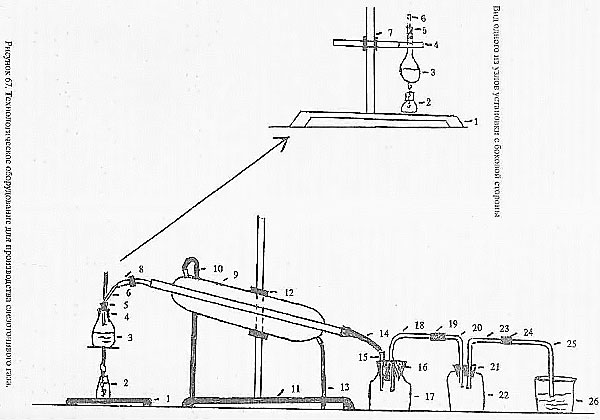
Рисунок из книги У. Паyэлла «Поваpенная книга анархиста» [4].
В настоящее время акролеин в промышленности получают путем каталитического окисления пропилена. В 1983 году мировое производство акролеина превысило 250 000 тонн[3]. Такое широкое распространение этого токсичного ирританта создает опасность его использования в террористических целях. Кроме того, акролеин легко получить даже в домашних условиях. Во времена СССР, когда свободная продажа газовых баллончиков населению была запрещена, акролеин, бром- и йодацетон изготавливались в домашних лабораториях химиками-любителями для применения в качестве самодельных «слезоточивых газов».
Симптомы отравления и токсичность. При кратковременном вдыхании небольших концентраций возникают жжение в глазах, слезотечение, конъюнктивит, отек век, чувство царапанья в горле и кашель. При воздействии более высокой концентрации явления раздражения выражены резче, могут присоединиться такие симптомы, как легкое головокружение, приливы крови к голове, боли в животе, тошнота, рвота, синюшность губ. В тяжелых случаях наблюдатся: замедление пульса, слюнотечение, похолодание конечностей, онемение кончиков пальцев, расширение зрачков и даже потеря сознания. Отмечались также состояние возбуждения, дезориентация в месте и времени. В легких случаях выздоровление через 1–2 дня, в более тяжелых — через 4–5 дней[21].
| Действие | Концентрация (мг/м3) |
Экспозиция |
|---|---|---|
| Порог восприятия запаха | 0,07 | — |
| Умеренное раздражение глаз | 0,6 | 5 мин |
| Раздражение глаз и носа | 2 | 2–3 мин |
| Непереносимая концентрация | 13 | 1 мин |
| Смертельная концентрация | 350 | 10 мин |
По данным Д. С. Синкувене (1970)[21]
После окончания Первой мировой войны в качестве возможного ОВ был изучался монохлоракролеин CH2=CCl–CHO, вызывающий слезотечение и образование пузырей.
Раздражающее действие акролеина обусловлено активацией TRPA1 - рецепторов, также как и других сенсорных ирритантов CN, CS и CR.
Галогенированные непредельные альдегиды
Кротоновый альдегид H3C–CH=CH–COH также является сильным лакриматором, но все же уступает по слезоточивому действию акролеину[9]. Он неоднократно рассматривался в качестве потенциального раздражающего ОВ как самостоятельного[17], так и в качестве растворителя для таких кристаллических ОВ, как хлорацетофенон. На расположенном ниже рисунке представлен прототип полицейской гранаты состоящей из двух стеклянных полусфер заполненных кротоновым альдегидом и тетрахлоридом кремния (SiCl4) и помещенных в металлический корпус. Добавление дымообразователя SiCl4 помогает контролировать область распространения слезоточивого дыма[18].
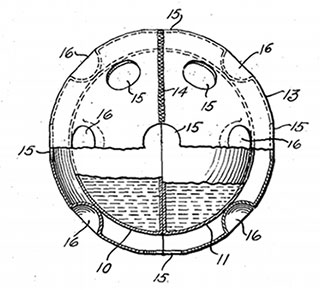
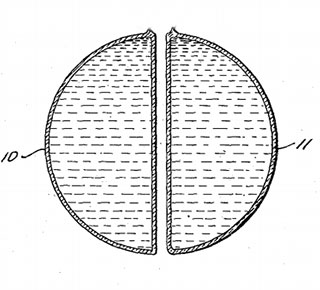
Кротоновый альдегид в раздражающих концентрациях не обладает выраженным токсическим действием и даже применяется в качестве одоранта — вещества, которое добавляют в бытовой газ для придания ему специфического запаха, предупреждающего об утечке[20].
Помимо кротонового выраженным раздражающим действием обладают пропионовый CH=CH–CHO и альфа-броммасляный альдегиды H3C–CH2–CHBr–CHO. Пропаргиловый альдегид HC≡C–CHO вызывает раздражение слизистых, которое, даже после кратковременного воздействии концентрации 22 мг/м3, продолжается больше часа[21].
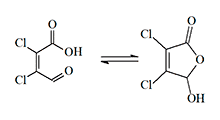
Очень сильным промышленным ирритантом является мукохлорная кислота, которая вызывает раздражение слизистых глаз и носа в концентрации 0,6–0,7 мг/м3 уже после нескольких вдохов, а попадание на кожу даже мельчайших частичек приводит к появлению эрозий и пузырей.
Еще больший интерес в качестве лакриматора представляет виниловый эфир мукохлорной кислоты синтезированный в годы Второй мировой войны. Это бесцветная, летучая жидкость обладает сильным слезоточивым действием, которое сопровождается слабостью, головокружением и шоковым состоянием.
 |
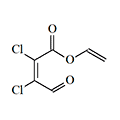 |
| Мукохлорная кислота | Винил мукохлорат |
Преимуществами этого ирританта считаются жидкое состояние, высокая летучесть при комнатной температуре, отсутствие запаха и большая продолжительность действия — от 30 минут до часа, даже после того, как человек покинет зону поражения. К недостаткам винил мукохлорида как лакриматора можно отнести 10-минутную задержку до начала слезоточивого действия и склонность к полимеризации[16].
Нитроолефины R–CH=CH–NO2 оказывают раздражающее действие на глаза при очень низких концентрациях, но из-за низкой устойчивости и склонности к полимеризации мало пригодны в качестве раздражающих ОВ[5]. 2-Нитро-2-бутен CH3–CH=CNO2CH3 вызывает у человека слезотечение в концентрации менее, чем 1:1 000 000[6].
Транс-β-хлоракринитрил Cl–CH=CH–CN и транс-β-бромакринитрил Br–CH=CH–CN относительно сильные раздражающие вещества, легко испаряющиеся при комнатной температуре, но такие же нестабильные как и нитроолфеины[7]. В качестве потенциальных лакриматоров также изучались 3-нитроакринитрил и 4-хлор-3-метил-3-бутен-нитрил.